Mölnlycke er klar til MDR
Den 25. maj 2017 trådte den europæiske forordning om medicinsk udstyr, 'MDR', i kraft, og erstattede direktivet om medicinsk udstyr, 'MDD'. Mölnlycke er godt forberedt til MDR-overgangen. Det interne MDR-overgangsprogram har været på plads siden september 2016 og arbejder på at sikre overholdelse af MDR-forpligtelserne. For at forblive på markedet skal klasse I ikke-sterile produkter være MDR-certificeret senest den 26. maj 2021, MDR-ansøgningsdatoen. Mölnlycke MDD-certificerede produkter af andre medicinske udstyrsklasser vil gå over til MDR inden udløbet af de respektive MDD-certifikater.
Mölnlycke MDR tidslinje
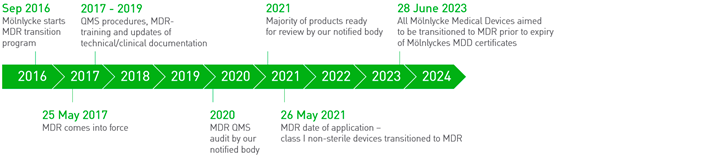
Mölnlyckes sortiment består af mere end 100 produktgrupper. Alle produkter i vores EU-sortiment vil blive MDR-certificeret inden udløbet af den respektive MDD-certificering, hvilket afhænger af klassificeringen af medicinsk udstyr. Klassificeringen af medicinsk udstyr for vores produkter ændres ikke med MDR.

De tre hovedformål med den nye forordning
- Forbedre sundheds- og sikkerhedsniveauet
- Fortsætte med at styrke den fri handel med medicinsk udstyr i EU
- Sikre, at produkterne er på højde med den nyeste teknologi og videnskabelige viden
Forordningen skulle være trådt i kraft i maj i år, men er blevet udskudt i ét år og vil træde i kraft den 26. maj 2021. Den absolut sidst dag, der kan sælges produkter, der kommer på markedet med MDD-certificering, er maj 2025.
Hvad er de største forskelle på MDD og MDR?
Et direktiv kan fortolkes forskelligt i hvert enkelt medlemsland, en forordning er meget mere omfattende. Der er forbedrede krav til sikkerheden og pålideligheden af medicinsk udstyr, med mere vægt på en livscyklustilgang, der er understøttet af kliniske data, samt øget overvågning efter markedsføring. De kompetente nationale myndigheder og EU-Kommissionen vil have en stærkere kontrol- og overvågningsrolle. Der er desuden tilføjet krav, der vil styrke gennemsigtighed og information for brugerne.
Resultatet vil i det lange løb være en stærkere, mere ansvarlig MedTech-industri, der favoriserer ansvarlige virksomheder.
Hvordan har MDR påvirket industrien?
MDR vil påvirke alt medicinsk udstyr, der sælges i EU, hvad enten det er fremstillet i EU eller importeret. Alt udstyr, herunder ældre produkter, skal recertificeres og have ny EU-certificering. Det kræves desuden af virksomheder, at de opgraderer og recertificerer deres kvalitetsstyringssystemer for at opfylde den ny forordning.
Den er bekostelig at implementere og kræver, at alt medicinsk udstyr skal have opgraderet teknisk dokumentation. Som resultat heraf forudsiges det, at mange eksisterende produkter ikke vil forblive på markedet.
I begyndelsen af april, mens Mölnlycke var i en stærk position, var der betydelig bekymring for, at indførelsen af MDR ville forværre manglen på personlige værnemidler (PPE) og andet medicinsk udstyr, der skulle bruges til bekæmpelse af coronavirus. EU-parlamentet er nu enedes om at udskyde skæringsdatoen for MDR med et år for at gøre det muligt for myndighederne og industrien at prioritere deres kræfter om COVID-19.
Udsættelsen var en lettelse for mange virksomheder, der ikke var så langt som Mölnlycke, og flere virksomheder vil nu være i stand til at opfylde kravene til tiden.
Hvad kan vores kunder forvente af den nye forordning?
Formålet med den nye forordning er i lighed med alle andre forordninger at skabe regler, der vil sørge for alles sikkerhed, både dem, der arbejder med produkterne, og patienterne, der bruger dem. Den nye forordning vil hjælpe sundhedspersonalet med at føle sig trygge ved at vide, at alle produkter, der er på markedet, efter at MDR er trådt i kraft, har været gennem en skrap vurdering og har et højt niveau af klinisk evidens.
Hvordan opfylder Mölnlycke tidsplanen for MDR?
Forsinkelsen af MDR har ikke haft indflydelse på Mölnlyckes arbejde med at opfylde den nye forordning. Vi var tidlige med at tage MDR til os og har allerede fået vores første udstedelse af MDR-certifikater, hvilket betyder, at vi allerede kan begynde at CE-mærke nogle af vores produkter i henhold til den nye forordning.
Vi er godt forberedt, og vores tidsplan følger stadig de oprindelige datoer for MDR. Vores kunder kan være sikre på, at vi vil fortsætte med at levere produkter med et højt niveau af beskyttelse af sundhed og sikkerhed, også efter at den nye forordning er implementeret.






